于康:肌肉衰减症临床诊疗及营养管理新进展
肌肉衰减症对人体健康有什么影响?
1989年,美国学者Irwin Rosenberg首次提出肌肉衰减症(Sarcopenia)的概念,它是指增龄相关的进行性全身肌量减少和(或)肌强度下降或肌肉生理功能减退。Sarcopenia会造成生活质量的下降,研究发现没有肌肉衰减的老年群体和有肌肉衰减者累计生存率的差别越来越大。
Sarcopenia具有持续性、广泛性和损害性。人体39岁开始肌肉衰减的速度可能会减慢,但不会停止。骨骼肌、内脏平滑肌、心肌都会随着年龄增长而衰减,其中心肌衰减还会伴随心率失常等问题,给身体造成损害。对于患有像糖尿病这样的慢性代谢性疾病的老人,他们的肌肉衰减是加速的。如果没有得到有效的诊断和干预,血糖控制不佳,这种加速就变得更快。
我们的研究表明,老年2型糖尿病患者的人体成分组织已经改变。包括骨骼肌在内的非脂肪组织出现了明显的下降,脂肪组织获得性增加,这些改变整体表现在体重增加,部分2型糖尿病老人还伴有肌肉衰减型肥胖。他们所有肌肉相关的指标,包括骨骼肌指数,骨骼肌数量都呈现明显的下降趋势。
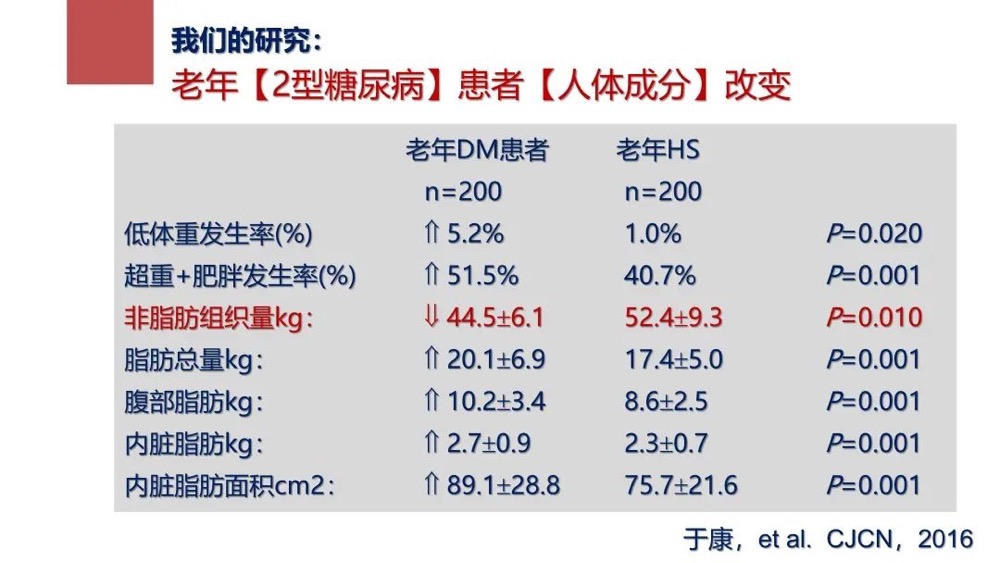
图1 老年2型糖尿病患者人体成分改变情况
老年2型糖尿病患者一旦患有Sarcopenia,临床结局会变坏,比如会增加术后并发症风险,出现肺部感染、胃肠炎、心力衰竭等一系列问题。
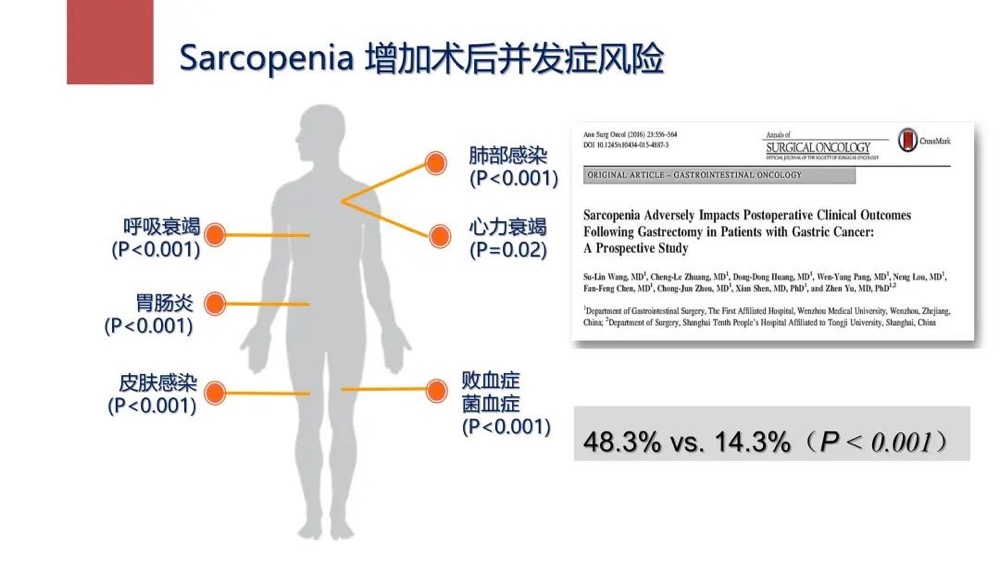
图2 肌肉衰减增加术后并发症的风险
我们团队一项纳入1.9万例研究对象的研究得出了两大结论。一是病人一旦患有Sarcopenia,综合性不良结局、跌倒、骨质疏松症、骨折和全因死亡出现的概率都会增加;二是患有Sarcopenia的门槛并不高,与性别、人种没有任何关系。
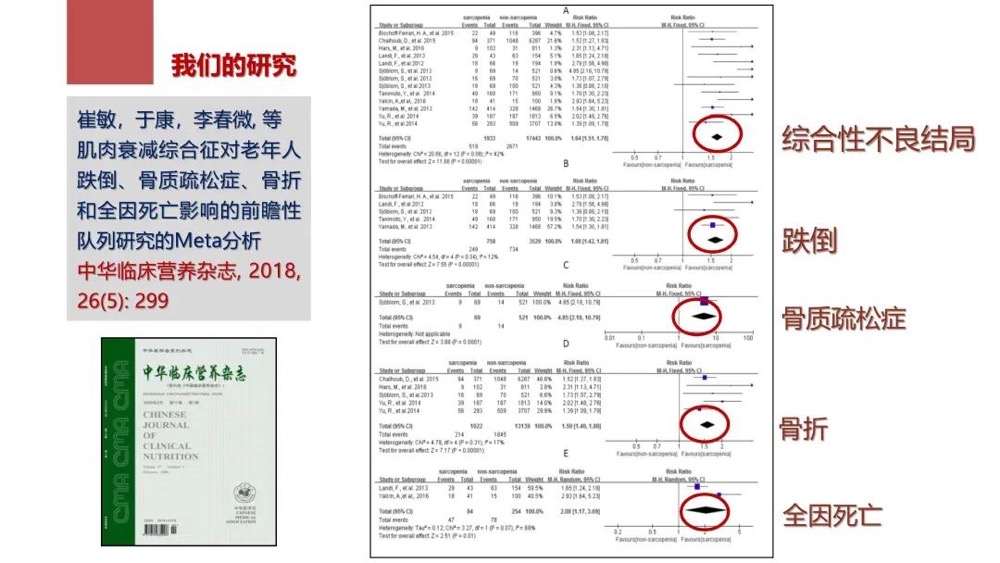
图3 肌肉衰减会提高老年人综合性不良结局和全因死亡的概率
对于诊断标准,无论按照哪种研究人员定义的标准,只要被诊断出Sarcopenia,患者的临床结局都会变坏。基于以上背景,2016年ICD-10(国际疾病分类)正式赋予Sarcopenia一个疾病代码。目前Sarcopenia中文译名有肌肉衰减症、肌肉衰减综合征、少肌症和肌少症。
肌肉衰减症是否“无药可治”?
2018年,欧洲老年人肌肉减少症工作组(EWGSOP)通过收集10年来积累的科学和临床证据,提出了三个重要的概念:第一,对肌肉衰减症的诊疗,应该贯穿于全生命周期;第二,通过早期有效的干预、预防可以延迟甚至可以逆转这种肌肉衰减;第三,在很多情况之下,肌肉力量和功能的下降要早于肌肉数量衰减而发生。
工作组还发布了新版EWGSOP2,将肌肉衰减定义更新为:仅有肌肉力量下降为可疑肌肉衰减症,若同时伴有肌肉质量和力量下降即可诊断为肌肉衰减症。上述两项加上躯体功能表现差可诊断为严重肌肉衰减症。值得关注的是EWSPOP2更强调通过临床路径来诊断,特别强调患者需要有一个自我评估,评估路径叫做F-A-C-S(Find-Assess-Confirm-Severity)。目前的评估方法,一是判断自己爬十级台阶时相较过去有没有更加困难,二是判断在客厅里搬几斤的重物,从墙角走到另一个房间角的时候,有没有感觉更加吃力,三是记录一年内不受外力影响下自己跌倒的次数有没有增加,之后还要结合专家的筛查,评定,诊断和严重性量化评估,来判断是不是真正患有Sarcopenia。
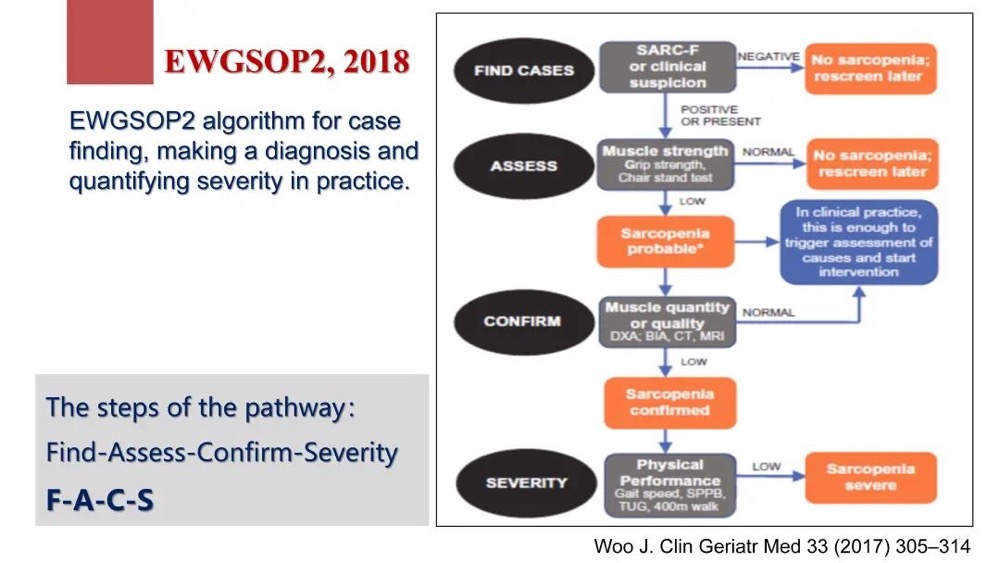
图4 EWGSOP2算法用于在实践中发现Sarcopenia病例、进行诊断和量化严重程度
相比之下,我们更强调把临床路径和SOP(标准操作程序)相结合起来诊断Sarcopenia,目前主要参考身体质量指数(BMI)和相对骨骼肌质量指数(RSMI),后者即为四肢骨骼肌的质量与身高平方的比值。当RSMI低于青年对照组两个标准差以上或者男性RSMI<7.0kg/m2、女性RSMI<5.5kg/m2时,即可判定为肌肉衰减症。
目前还没有特定的有效药物和临床治疗手段对抗Sarcopenia,我们和中国科学院也在合作探索用药物干预的可能性,但是到目前为止所有的研究结果都是不尽如人意的,很多研究甚至中断了。基于以上原因,大家开始从营养和运动角度研究干预Sarcopenia的方法。
肌肉衰减症目前唯一有效的干预方法——<营养+运动>为基础的生活方式
通过进行流行病学的调查,建立健康队列,我们团队现在得出了一些结论:一是65岁以上人群现患率明显比总人群现患率高;二是女性现患率比男性高,女性人群更可能出现前期病变,患有重症Sarcopenia的风险也更高;三是无论按照哪种诊断标准,65岁以上人群患有肌肉衰减性肥胖的概率会提高。
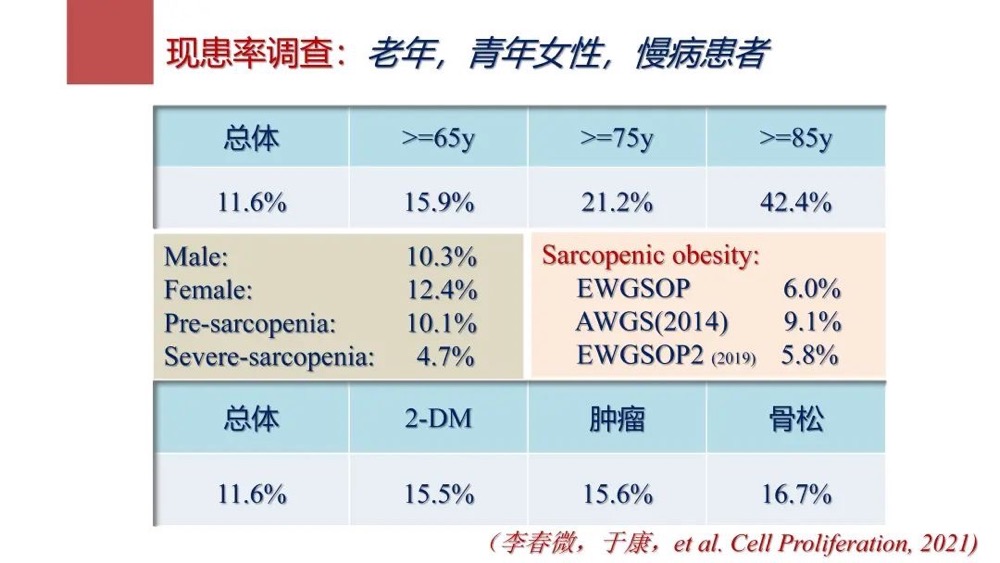
图5 于康团队对老年、青年女性和慢病患者的肌肉衰减症现患率调查
有关肌肉衰减的影响因子很多,研究发现随着年龄的增加,独居、营养不良、大量吸烟、缺少抗阻运动都会提高老人患有肌肉衰减症的概率。我们团队把年龄、握力、BMI和小腿围合成了一个PUMCH index(协和指数),用这个指数作为下一期筛查和评定Sarcopenia的依据。

图6 于康团队采用的PUMCH index(协和指数)
Sarcopenia老年患者血清里的部分炎症因子会显著升高或者降低:TWEAK叫做肿瘤坏死因子样弱凋亡诱导因子,与肌肉衰减呈负相关关系;IGF-1叫做类胰岛素生长因子,与肌肉衰减呈正相关关系。这些炎症因子与很多慢性病(糖尿病等)的产生有着很大的关联,如果过高会严重影响慢病群体的健康。
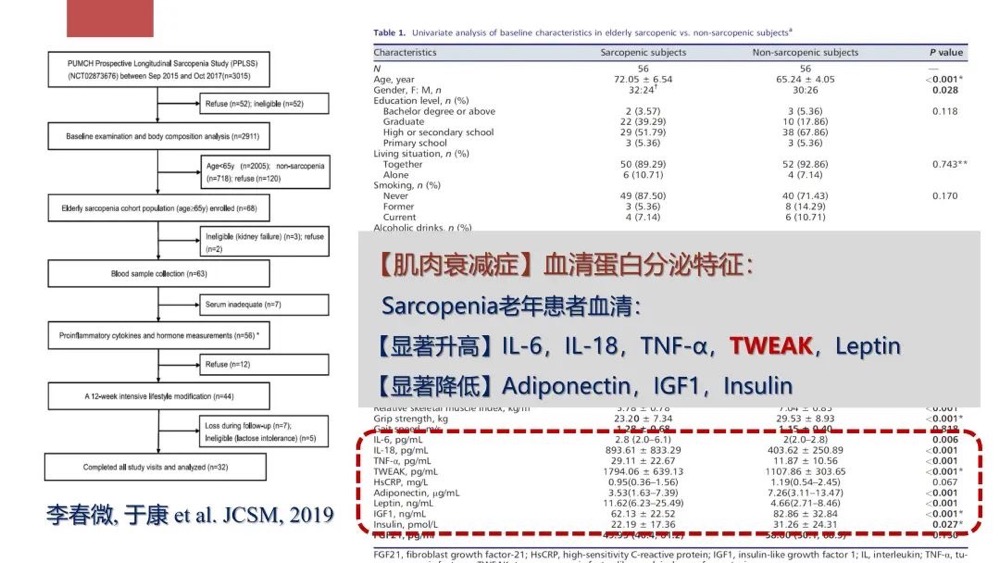
图7 肌肉衰减症对促炎因子的影响
我们对中老年肌肉衰减症患者进行了12个星期的干预,干预方式采取非药物手段,以乳清蛋白为主体进行营养补充,再加上以抗阻训练为基础的运动干预。干预结果都向着有利于肌肉恢复的方向发展,包括肌肉重量的增加。只是患者的步速还没有提高理想水平。总体来讲,患有肌肉衰减症的中老年人,通过一定程度的营养方式干预,就可以获得肌肉状况的改善。
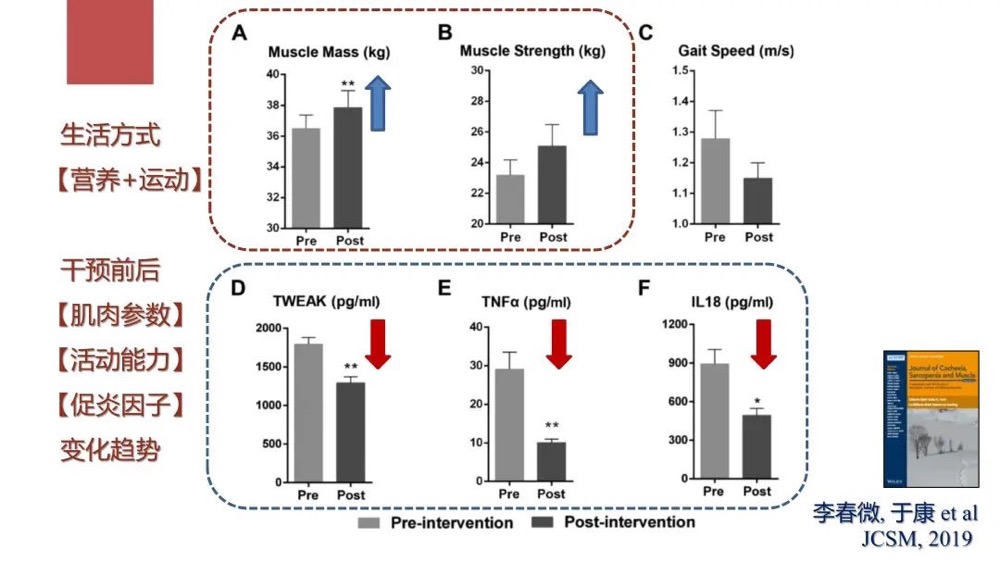
图8 营养+运动干预前后,肌肉参数、活动能力和促炎因子的变化趋势
目前的问题是,Sarcopenia患者的肌肉维护成本太高。一旦干预停止,患者的肌肉状况就会回到干预前的水平。营养管理既要有安全性,又要有可行性,中老年患者只有彻底改变生活方式,才能获得肌肉状况的持续改善。
营养+运动?单纯营养?单纯运动?
我们团队发现补充营养加运动,或者单独补充营养都能有效的改善肌肉的数量和力量,单独的补充营养还能减少过度的脂肪堆积,即使是那些运动不方便或者不敢运动的老年人,他们一样可以通过饮食来得到改善肌肉的机会;单独的运动干预效果不确定。

