干预阿尔茨海默症有了新策略——补充全植物食品
我国有约千万阿尔茨海默症患者
随着我国人口老龄化日益加剧,老龄人口的健康问题不容忽视。阿尔兹海默症(Alzheimer's disease,AD)是老年痴呆中最主要的形式,主要表现为认知功能下降、精神状态和行为障碍、日常生活能力逐渐下降等。截止2019年,全球已有约5000万阿尔兹海默症病例;预计到2050年,病例数将达到1.52亿例,是威胁老年人健康的“第四大杀手”。我国也有类似的情况。国家统计局数据显示,中国60岁及以上人口持续增长,截止到2020年人口普查时,60岁以上老龄人口已达到2.6亿。其中有1507万痴呆患者,而阿尔兹海默症患者就达983万。因此,与衰老密切相关的阿尔兹海默症将给社会带来严峻的经济负担。阿尔兹海默症的主要病理特征是淀粉样蛋白β (Aβ)斑块的沉积和由tau蛋白形成的神经原纤维缠结。然而,经典的Aβ和tau理论并不能完全解释阿尔兹海默症的发病机制。

图1 广东省科学院微生物研究所吴清平院士团队与暨南大学丁郁研究员团队近日在《Critical Reviews in Food Science and Nutrition》上发表的相关研究《全植物食品及其大分子:调节阿尔兹海默症中神经炎症的新策略》
研究阐释干预阿尔茨海默症新途径
研究发现,神经炎症甚至发生在阿尔兹海默症经典生物标记物和认知障碍之前。炎症因子不仅能通过上调β分泌酶的表达促进Aβ产生,还能促进tau蛋白磷酸化和扩散,进而引发阿尔兹海默症并加速其发展。神经炎症被定义为继发于神经元损伤的中枢神经系统(central neuronal system,CNS)中的炎症反应。星形胶质细胞和小胶质细胞是中枢神经系统炎症反应的靶点,激活小胶质细胞中的神经炎症主要受脂氧素A4(LXA4)-转录因子核因子-κB(NF-κB)和丝裂原活化蛋白激酶(MAPK)信号通路的调节。在正常情况下,NF-κB与其细胞质内的抑制蛋白κB(IκB)结合,处于非活动状态。一旦被激活,IκB被降解,NF-κB易位进入细胞核,进行促炎因子的转录。而作为炎症反应的一种内源“刹车信号”,LXA4可以抑制NF-κB信号通路的激活。同时,c-Jun NH2-末端激酶(JNK)和p38 MAPK可以通过激活活化蛋白-1(AP-1)来促进促炎因子的转录。因此,抑制神经炎症可以成为预防/治疗阿尔兹海默症的新途径。
以植物食品为主的健康饮食模式可以预防和改善认知障碍
尽管现代医学进步卓越,但目前仍然没有有效的药物可用来治疗阿尔兹海默症。因此,迫切需要寻找低副作用的天然活性物质来预防或延缓阿尔兹海默症的发生发展。全植物食品作为维持和改善健康的营养来源受到消费者的高度认可。研究表明,在动物模型和临床实验中,膳食补充全植物食品如蘑菇、浆果、姜黄和大蒜等,可以通过调节LAX4-NF-κB或/和MAPK两条信号通路来抑制神经炎症,进而改善认知障碍(见图2)。
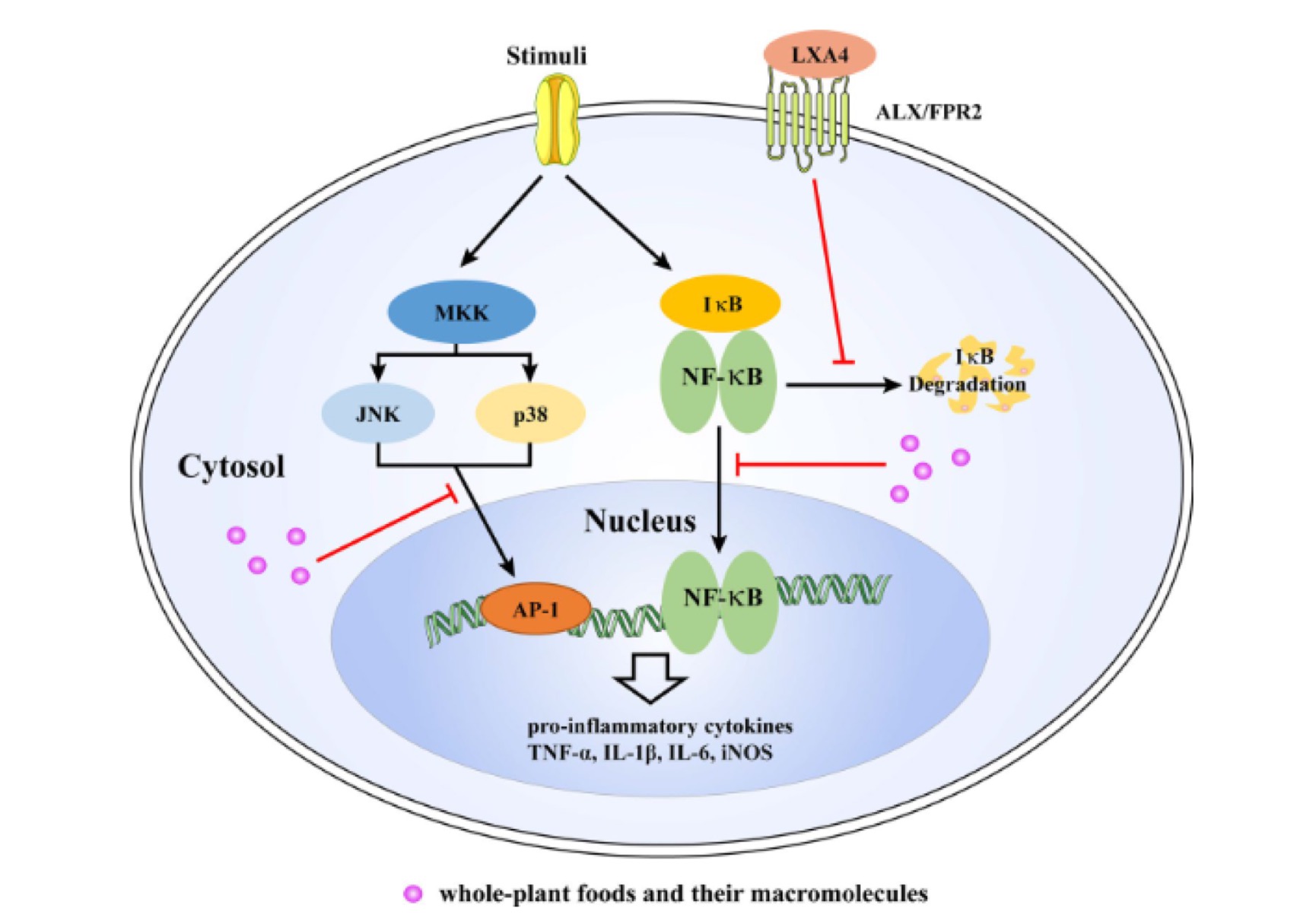
图2 全植物食品及其大分子调节神经炎症的关键信号通路
全植物食品对神经炎症的改善主要归功于其中的功能性大分子,如多糖、多酚和多肽。多糖的糖苷键、多酚的官能团和多肽的氨基酸个数等都会影响其活性。同时,在全植物食品中不同成分之间的相互作用可能会产生协同/拮抗效果,然而这些成分间的相互作用在抗神经炎症活性方面研究较少,需进一步深化。在日常生活中,人们往往同时摄入多种食物,而非单纯地补充某一类食物。研究发现,膳食习惯也与阿尔兹海默症的发生有关。例如遵循地中海饮食(Mediterranean diet,MeDi),控制高血压饮食(Dietary Approach to Stop Hypertension,DASH),和这两种饮食模式的衍生形式地中海-DASH干预退行性疾病饮食模式(Mediterranean-DASH Intervention for Neurodegenerative Delay,MIND),都可以有效降低认知衰退的风险。这三种饮食模式都倡导多食用蔬菜、水果、豆类和谷物,少食用红肉和乳制品。蔬菜水果中大量的维生素、多糖和多酚等,坚果和豆类中含有大量的多肽等活性物质都使得这些食物具有优良的活性。
要调节中枢神经系统中的神经炎症,全植物食品和活性大分子必须先通过血脑屏障。虽然部分疏水性物质可通过被动运输及一些亲水性物质可通过特定受体通过血脑屏障,但绝大部分天然活性物质仍存在生物利用度低、易降解和靶向性低等问题。一些新的分子工程技术已被用于克服这些限制。由于尺寸小、颗粒形状多样和靶向运输配体等优点,纳米颗粒运载已被广泛研究用于如多肽和多酚等生物活性成分的递送。靶向递送有效地提高了正常摄食中生物活性成分的生物可及性和利用度,从而提供了显著的疗效。此外,纳米颗粒在其表面被目标特异性配体或抗体功能化,使生物活性成分无需扩散即可直接到达特定的作用位置。因此,基于纳米颗粒运载活性物质的方法可能是改善全植物食品或大分子拮抗神经炎症应用的理想方式。除了直接作用于靶标外,活性大分子还可以改变肠道微生物的组成并进一步产生有益的代谢物,从而通过肠-脑轴调节神经系统(见图3)。从活性物质和肠道微生物互作的角度,寻找具有活性的有效代谢物,也为揭示活性大分子作用机制提供了新思路。
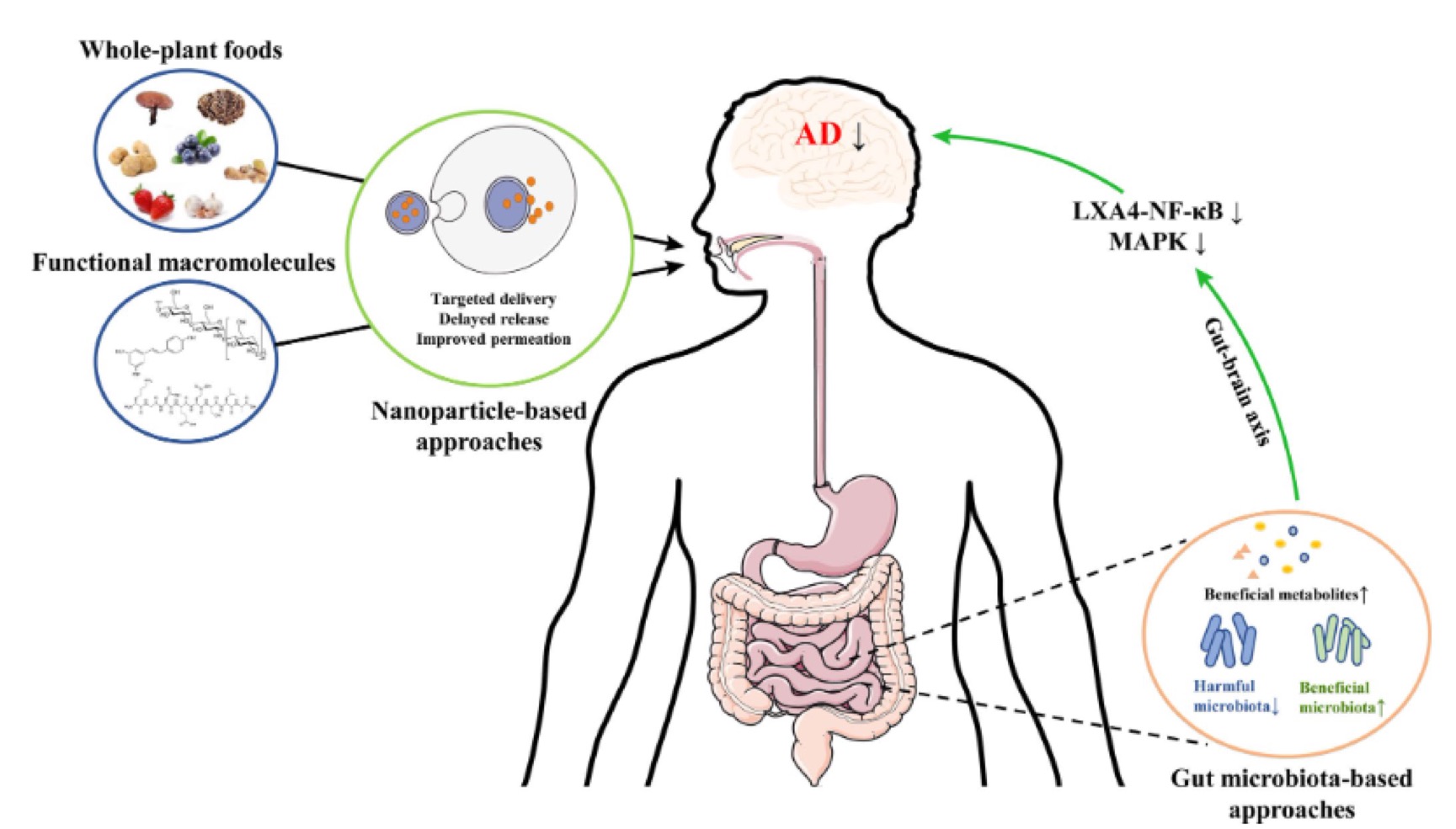
图3 全植物食品和活性大分子改善神经炎症的方式
个人总结
总之,神经炎症被认为是阿尔兹海默症的主要驱动因素。参与调节神经炎症的主要信号通路LAX4-NF-κB和MAPK是全植物食品和/或生物活性化合物发挥作用的关键。食用全植物食物,如蘑菇、浆果、姜黄和大蒜,可以通过调节信号靶标有效改善神经炎症,因此可作为预防阿尔兹海默症发生发展的推荐饮食模式。全植物食品对神经炎症的调节作用归功于多糖、多酚和多肽三种主要的生物活性成分。因此,挖掘具有抗神经炎症的天然活性产物将成为干预阿尔兹海默症的新途径,具有广阔的发展前景。
作者介绍
丁郁,博士,研究员,博士生导师,国家级人才支持计划入选者,广东省“丁颖”科技奖获得者,暨南大学“彭磷基青年讲席”教授,广东省“微生物安全与健康”重点实验室副主任,广东省科学院微生物研究所及华南应用微生物国家重点实验室客座研究员。主要研究方向包括:食品微生物安全、植源性功能性食品研发、生物反应器等。近五年主持了包括国家重点研发计划在内的多项国家级及省部级科研项目,迄今发表SCI论文100余篇,申请国家发明专利40余件,获授权6件。
参考文献
Huang R , Zhu Z, Wu Q , et al. Whole-plant foods and their macromolecules: untapped approaches to modulate neuroinflammation in Alzheimer’s disease[J]. Critical Reviews in Food Science and Nutrition, Published online: 23 Sep 2021. doi:10.1080/10408398.2021.1975093

