发芽糙米替代精米可有效改善糖尿病患者代谢紊乱
谷物是重要的膳食组成部分,是人体重要的能量来源。根据加工程度不同,谷物可分为精制谷物和全谷物。中国营养学会团体标准T/CNSS008-2021《全谷物及全谷物食品判定及标识通则》明确了全谷物、全谷物食品的判定技术要求及标签标识,其中发芽糙米就属于全谷物。与精制谷物相比,全谷物和全谷物食品保留了谷物原料中更多的天然营养成分。中国健康与营养调查(CHNS)最新数据显示,中国成年人的平均全谷物摄入量为14.2g,仅占总谷物摄入量的3.0% ~7.0%。这意味着只有7.0% ~17.2%的中国居民能够达到膳食指南推荐的50g/天的最低标准。相关研究[1]显示高精制谷物(≥2份/天)摄入与代谢综合征的高风险相关(男性- HR:1.21; 95% CI: 1.04, 1.41; P = 0.012; 女性-HR: 1.43; 95% CI: 1.23, 1.66; P<0.0001)。
近日,温州医科大学单毓娟团队在Clinical Nutrition上发表了发芽糙米替代等量精制谷物对2型糖尿病患者代谢改善的研究结果。

研究背景及方法
2型糖尿病(T2DM)是世界上增速最快的慢性非传染性疾病之一,并发症累及全身多个脏器组织。据国际糖尿病联合会(IDF)预计,全球T2DM患病率将在2030年增加25%,2045年增加51%。2015~2019年期间,我国T2DM总体患病率高达14.92%[2]。老龄化加剧、超重和肥胖率持续增高、膳食结构不合理,以及体力活动的缺乏都将继续威胁T2DM的发生发展。
发芽糙米(GBR)在萌发过程中,大量残留酶被激活,不仅显著改善糙米的口感,还产生多种有益活性产物,如γ-氨基丁酸(GABA)、维生素E等,这些活性产物可能有助于改善T2DM、高血压、高脂血症患者的代谢紊乱。本研究招募了220名T2DM患者,根据纳入和排除标准筛选后,共99名患者参与了本项随机对照干预试验,对照组(45名)维持原有饮食习惯不变,即主食以精制大米为主,干预组(54名)用100g/天的GBR替代原有饮食中的精制谷物,干预3个月,最终43名对照组和42名干预组参与者完成了基线、第一个月、第二个月、第三个月结束时的FFQ调查和血清样本采集;通过对血糖、血脂、饮食炎症指数以及血清脂肪酸代谢组学、n-3和n-6多不饱和脂肪酸(PUFA)相关代谢产物的测定和分析,从炎症角度探索GBR干预对T2DM患者血糖血脂紊乱的改善作用。
与精米相比,发芽糙米的大部分营养物质含量较高
植物性食物营养成分组成受环境、地域影响较大,为了更好的分析GBR改善糖脂代谢的机制,对本实验提供的GBR和本地的精米进行了主要营养成分检测,GBR有更高的膳食纤维、维生素B1、维生素B6、维生素E、烟酸、钙、镁、锌、GABA、阿魏酸(FEA)含量(图1),且主要差异营养素均具抗炎潜力(炎症效应指数均<0)。
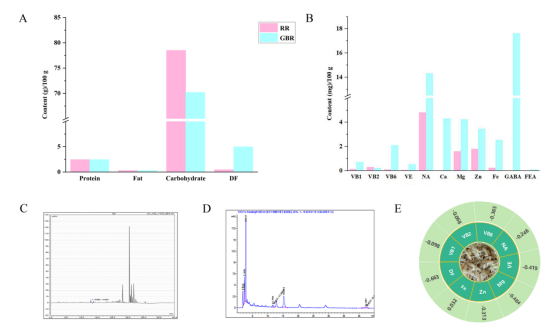
图1. 精制大米(RR)和GBR多种营养成分含量的比较。A.宏量营养素; B其他成分; C. GABA 与烟酸(NA)液相色谱图; D. VB6 液相色谱图; E炎症效应指数
GBR通过抗炎改善T2DM患者的代谢紊乱
计算两组在基线和干预结束时的膳食炎症指数(DII),并检测血清样本的TC,TG, HDL, LDL, FBG, HbA1c水平。发现干预后,GBR组患者DII明显低于对照组,且膳食纤维和维生素E摄入量显著高于对照组,同时FBG, HbA1c, TG水平显著降低,HDL显著升高(图2),且脂质代谢的改善更为显著。相关性分析结果显示FBG,HbA1c与DII呈正相关, HDL与DII呈明显的负相关(图3),提示GBR具有更好的抗炎潜力,且能有效降血糖、降血脂,但GBR是如何影响脂代谢,如何发挥抗炎作用,从而改善糖尿病患者代谢紊乱,尚不清楚。
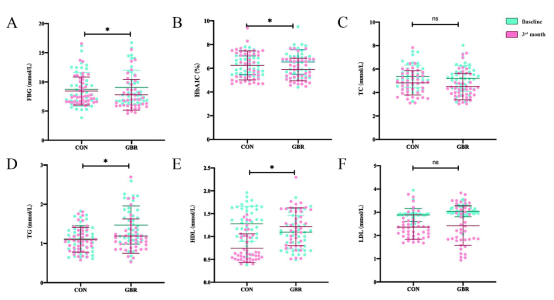
图2. 各组血糖、血脂相关参数的变化
注:ns,无统计学意义。对CON组**P<0.01,*P<0.05
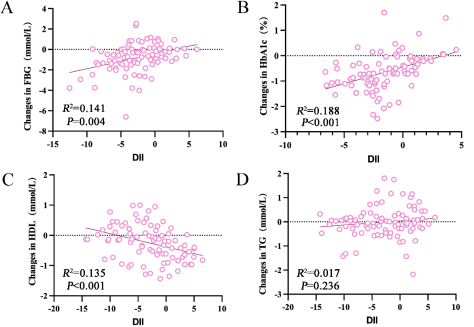
图3. 糖尿病风险与营养炎症指标相关性分析
GBR能够有效提高n-3 PUFA水平
本研究进一步探讨了GBR改善血糖、血脂的机制,对血液样本进行靶向脂肪酸谱检测,收集并分析了19种主要脂肪酸的含量数据。尽管脂肪酸在各组中的整体分布无明显差异(图4),但与对照组相比,GBR干预后患者油酸(C16:1,n-9),α-亚麻酸(C18:3,n-3),EPA(C20:5,n-3)显著升高,提示GBR能有效提高n-3 PUFA水平,明显改变受试者的血清脂肪酸构成。GBR组SFA含量较基线相比显著降低,且降幅较对照组更明显(图5A)。GBR组不饱和脂肪酸(UFA)和n-3 PUFA百分比均高于基线水平,且较对照组增加更显著(图5B-5C)。然而,GBR与对照组之间n-6 PUFA百分比差异不明显(图D),但n-3/n-6 PUFA显著升高。这些结果提示GBR干预降低了血清SFA含量,增加了UFA和n-3 PUFA含量,并改善n-3与n-6 PUFA的平衡。
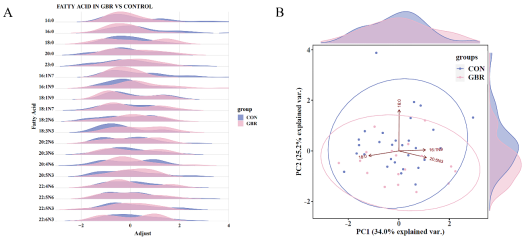
图4. 标准化脂肪酸的分布及方差分析。A.标准化脂肪酸含量分布; B.脂肪酸主成分分析(PCA)
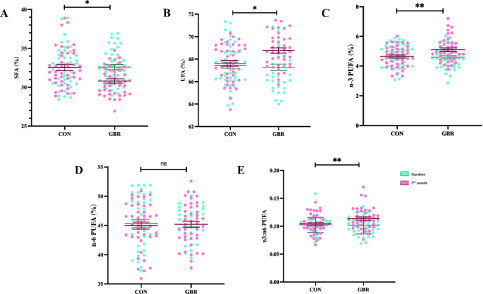
图5. 干预前后T2DM患者脂肪酸含量的变化。A.血清总饱和脂肪酸(SFAs)百分比变化; B.血清总不饱和脂肪酸(UFA)百分比; C.血清总n-3 PUFA百分比; D.血清总n-6 PUFA百分比;E.血清总n-3/n-6 PUFA百分比;ns,差异无统计学意义;与CON组相比,**P<0.01, *P<0.05
GBR通过影响n-3和n-6代谢物抗炎,改善血糖血脂水平
研究发现,干预3个月后,GBR组血清消退素E1(RVE1)、促炎症消退介质Maresin1(Mar1)、程序性死亡受体1(PD1)水平均显著升高,且高于对照组(图6C-6E)。血清消退素D1(RVD1)水平无变化,对照组白三烯B4(LTB4)、前列腺素E2(PGE2)升高,GBR组略有下降(图6A、6B)。血栓素B2(TXB2)未见变化。这些数据提示,GBR干预可以通过增加T2DM患者n-3 PUFA代谢产物RVE1、Mar1、PD1,减少T2DM患者n-6 PUFA代谢产物LTB4、PGE2的产生来减轻炎症效应。这些结果表明GBR干预能有效增强n-3 PUFA代谢,从而发挥抗炎作用。通过进一步的关联分析发现,PD1的变化与FBG呈负相关,而T2DM患者血清Mar1、RVE1、PD1的变化与血清HDL呈正相关。这些结果表明,GBR可能通过影响n-3和n-6代谢物来抗炎,从而改善血糖血脂水平。
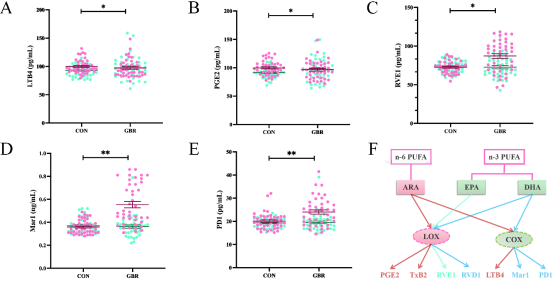
图6. n-3和n-6脂肪酸炎症相关代谢产物的变化。A-E.血清LTB4, PGE2, RVE1, Mar1, PD1含量;F. n-3和n-6脂肪酸炎症相关代谢网络图; **P<0.01, *P<0.05

图7. 脂肪酸(A)及其代谢产物(B)与糖尿病风险的相关性分析
文章结论
发芽糙米干预(100g/天)可能通过增强n-3代谢,改善血清脂肪酸构成,发挥抗炎作用,改善T2DM人群糖脂代谢异常(图8)。
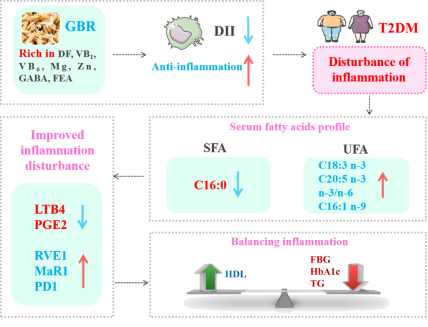
图8. GBR干预对2型糖尿病人群糖脂代谢影响的作用概述
作者评述
本研究是在我国东北地区进行的第一个以GBR替代部分精制谷物,对T2DM患者(n=85)脂肪酸代谢影响的RCT研究。GBR通过增加n-3 PUFA代谢(RVE1、PD1和MaR1)和减少n-6 PUFA代谢(LTB4和PGE2)发挥良好的抗炎作用,这一点值得进一步的探索和研究。
但该研究仍存在一定的局限性:首先,该研究不能设计为双盲试验;其次,该研究的参与者可能患有严重的糖尿病,因此他们可能不能代表标准的糖尿病患者。最后,干预样本量较少,且干预人群主要来自东北地区哈尔滨市的中心区域,因饮食和生活环境等的差异,研究结果可能不能应用于中国其他区域,未来应该开展更大规模的GBR干预研究。
作者简介
单毓娟教授,温州医科大学教授、教学名师、博士研究生导师。兼任中国营养学会营养转化分会副主任委员、中国营养学会膳食与烹饪营养分会常务委员。主持国家自然科学基金4项;省部级及海外合作项目6项。发表SCI论文50余篇。获国家授权发明专利1项;获第二届全国高校教师教学创新大赛二等奖;中华预防医学会二等奖、省政府一等奖和二等奖等。
参考文献
[1] Kang Yunhee, Lee Kyueun, Lee Jieul, Kim Jihye, Grain Subtype and the Combination of Grains Consumed Are Associated with the Risk of Metabolic Syndrome: Analysis of a Community-Based Prospective Cohort. J Nutr. 2020, 150, 118-127.
doi: 10.1093/jn/nxz179.
[2] 首部中国糖尿病地图要点速览,郭立新,2022北大医院内分泌代谢疾病规范化诊疗论坛
[3] Guanqiong Na, Jing Zhang, Dian Lv, et al. Germinated Brown rice enhanced n-3 PUFA metabolism in type 2 diabetes patients: A randomized controlled trial[J]. Clinical Nutrition, 2023,42(4):579-589.
doi: 10.1016/j.clnu.2023.02.001.

